Un gas perfetto monoatomico percorre un ciclo termodinamico composto da quattro trasformazioni successive:
AB: isoterma da VA a VB alla temperatura T1;
BC: adiabatica da B a C con VB minore di VC e temperatura finale T2;
CD: isoterma da C ad A con VA minore di VC;
DA: isocora per tornare al punto A.
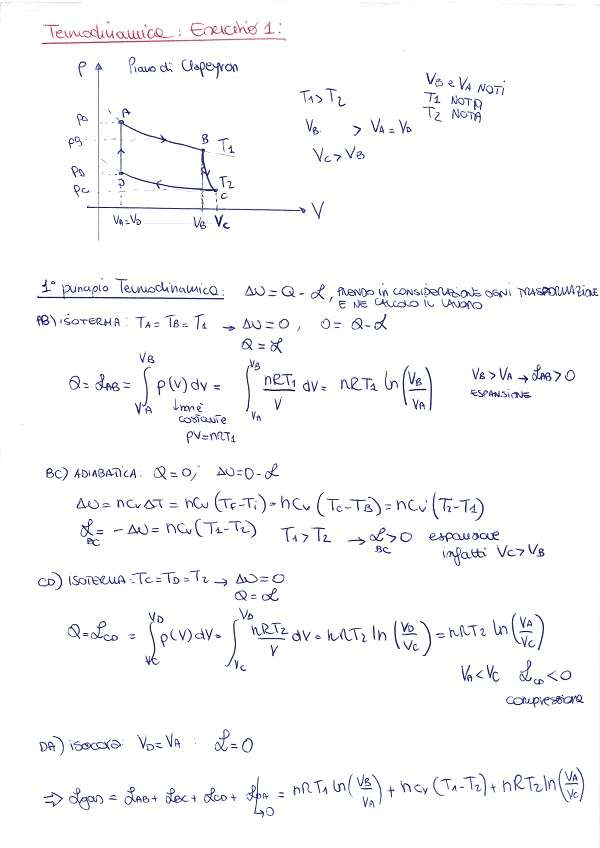
Dopo aver disegnato il ciclo sul piano di Clapeyron, ricavare il lavoro totale compiuto dal gas. (Considerare come dati noti: VB, VA, T1 e T2).

ciao, ma il lavoro da C a D non era negativo??nel lavoro finale quindi devo sottrarlo non sommarlo giusto?
Manca il numero di moli
L’esercizio è chiarissimo. Ma come faccio a capire che T1>T2?
Devi guardare i fasci di isoterme, ovvero i rami di iperbole.
A e B si trovano sullo stesso ramo, e dunque sono alla stessa temperatura, T1.
C e D si trovano su un ramo più “interno” (più vicino all’origine), a temperatura più bassa.
La temperatura aumenta man mano che ci si allontana dall’origine, diminuisce man mano che ci si avvicina all’origine.